Gene , die die Gesundheit regelt der Kraftpaket Zelle könnte Ziel für die Entwicklung neuer Diabetes-Medikamenten sein
Ein Team von Forschern der Perelman School of Medicine an der University of Pennsylvania führte gestellt, dass ein Gen die Anfälligkeit für Diabetes Typ 1 regelt Selbstzerstörung der Energiefabrikder Zelle. Sie berichten ihre Ergebnisse in dieser Woche in Cell.
Der Weg im Mittelpunkt dieses Gen könnte zur Vorbeugung und Kontrolle von Diabetes Typ 1 ausgerichtet sein und können zur Behandlung von anderen metabolischen assoziierten Krankheiten erstrecken .
Das Team fand heraus , dass das Gen , Clec16a , wenn in Pankreaszellen , ist für den normalen Glukose -stimulierte Freisetzung von Insulin erforderlich ist. Darüber hinaus haben Personen mit einer Variation in der Gensequenz in der Nähe Clec16a Expression des Proteins in der Inselzellen reduziert und somit die Insulinsekretion reduziert.
Erstautor Scott A. Soleimanpour , MD, ein Postdoctoral Fellow im Labor von Co- Senior-Autor Doris Stoffers , MD, PhD , Professor für Medizin, arbeitete diese Rolle Clec16a in Betazellen der Bauchspeicheldrüse . Soleimanpour ist jetzt Assistant Professor an der University of Michigan Medical School. Stoffers ist auch Mitglied des Instituts für Diabetes, Übergewicht und Stoffwechsel an der Penn .
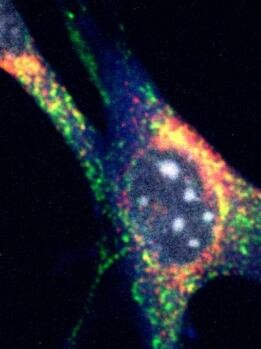
Maus-Fibroblasten zeigt Clec16a (rot), das Lysosom Protein Lamp1 (grün), die Autophagosom Protein LC3 (blau) und DNA (grau). Die gelbe Überlappung der roten und grünen Flecken zeigt, dass Clec16a besteht in der endosomalen Kompartiment , ein Teil des zellularen Systems zur Entsorgung mitophagy verwendet .
Bildnachweis: Scott Soleimanpour , MD ( University of Michigan Medical School ) und Doris Stoffers , MD, Ph.D. ( Perelman School of Medicine )
Die Selbstzerstörung Prozess der Energiefabriken( Mitochondrien) der Zelle wird als mitophagy . Dies bedeutet wörtlich die Selbst Essen von Mitochondrien, die Standorte für die Herstellung der Energie-Molekül ATP . Betazellen in der Bauchspeicheldrüse in Mitochondrien aufgrund ihrer Insulin absondernden Funktion eines energieintensiver Prozess angereichert .
Mitophagy beinhaltet den Abbau und Recycling von weniger gut funktionierenden, alten Mitochondrien an die frische zu bauen . Clec16a steuert Beta- Zell-Funktion in dieser Entsorgungsweg und ist gedacht, um mit Diabetes verbundene mitophagy verhindern.
War wenig über die Funktion des Clec16a Protein in Säugetieren oder auf ihre Rolle bei der Einleitung der Erkrankung bekannt. Das Team fand heraus , dass Clec16a interagiert mit einem Enzym namens Nrdp1 , die durch ein anderes Protein namens Parkin funktioniert. Normalerweise Parkin regelt mitophagy indem zunächst Tagging ungesunde Mitochondrien zur Entsorgung bringen.
Mäuse mit einem Pankreas - spezifischen Deletion von Clec16a haben abnorme Mitochondrien , die weniger ATP , die für die normale Funktion der Betazellen und letztlich Insulinsekretion erforderlich zu produzieren. Insbesondere stellten sie fest, dass der Verlust der Clec16a führt zu einer Erhöhung in Parkin ein Hauptregulator der mitophagy . Was mehr ist, fand das Team heraus , dass die endgültige Beseitigung von ungesunden Mitochondrien war auch defekt.
"Das ultimative Ergebnis der Löschung von Clec16a ist eine Ansammlung von ungesunden Mitochondrien , was zu weniger Insulin durch die Betazellen abgesondert ", sagt Stoffers .
Koautoren von der Universität Lund und Skåne Universitätsklinik in Schweden ein Panel von menschlichen Inselzellen , die Soleimanpour zu bestimmen, ob eine kleine Diabetes - Risiko Variation in der DNA-Sequenz in der Nähe des Clec16a Gen direkt betroffen das Gen die normale Expression und Funktion erlaubt. Personen mit dieser kurzen Sequenzvariante hatte Clec16a Expression in Inselzellen sowie leicht erhöhter Blutzucker verringert. Darüber hinaus erschließt eine große, bisher veröffentlichten genetischen Datenbank ermöglichte es den Forschern , um die gleiche Krankheit assoziierte Sequenzvariante mit reduzierten Betazellfunktion weiter zu korrelieren. Daraus wird der Schluss gezogen, dass die Mannschaft in einem normalen Zustand befindet, steuert Clec16a Betazellfunktion und verhindert Diabetes durch Steuern mitophagy .
"Im Jahr 2007 unsere Genomik Team fand das erste Gen in einer genomweiten Suche auf eine wichtige Rolle bei Diabetes Typ 1 zu spielen, aber wir haben nicht die Funktion weiß", sagte Co- Senior-Autor Hakon Hakonarson , MD, PhD , Direktor der das Zentrum für Angewandte Genomik am Kinderkrankenhaus von Philadelphia. "Jetzt verstehen wir, wie dieses Gen spielt eine entscheidende Rolle bei der Regulierung der Insulin-Stoffwechsel . "
Der Roman Clec16a Weg könnte für die Prävention und Kontrolle von Diabetes ausgerichtet werden und zur Pathogenese anderer Clec16a und Parkin -assoziierten Erkrankungen zu verlängern, folgern die Forscher.